Theo GLOBOCAN 2022, toàn thế giới ước tính có gần 20 triệu ca ung thư mới và hơn 9,7 triệu ca tử vong, trong đó, 3 loại ung thư hàng đầu theo số ca tử vong gồm ung thư phổi, vú, đại trực tràng. Tại Việt Nam, thống kê có hơn 180.000 ca mắc mới và hơn 120.000 ca tử vong do ung thư.
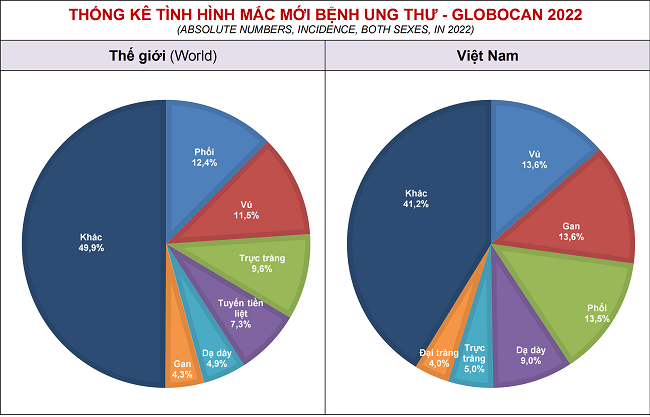
* https://gco.iarc.fr/today/en/dataviz/pie?mode=population&group_populations=0
Kĩ thuật sinh thiết mô (tissue biopsy) khối u là “tiêu chuẩn vàng” trong chẩn đoán ung thư, tuy nhiên, kĩ thuật này yêu cầu bệnh nhân tuân thủ quy trình trước, trong và sau khi lấy mẫu. Trước khi thực hiện lấy mẫu sinh thiết, chỉ định xét nghiệm có thể sẽ yêu cầu kiêng ăn và xét nghiệm dị ứng các chất trong thủ thuật. Trong khi thực hiện sinh thiết, do là kĩ thuật xâm lấn nên bệnh nhân được gây tê, sinh thiết kim là gây tê tại chỗ, với sinh thiết nội soi hoặc cắt bỏ mô và vị trí khó sinh thiết là gây tê toàn thân. Quá trình này diễn ra từ vài phút tới vài giờ đồng hồ, sau đó, phải yêu cầu theo dõi bệnh nhân và hàng loạt quy trình xử lí mẫu sau khi sinh thiết. Do vậy, về cơ bản, sinh thiết mô có thể gây đau, chảy máu, biến chứng cho bệnh nhân và mất nhiều thời gian.
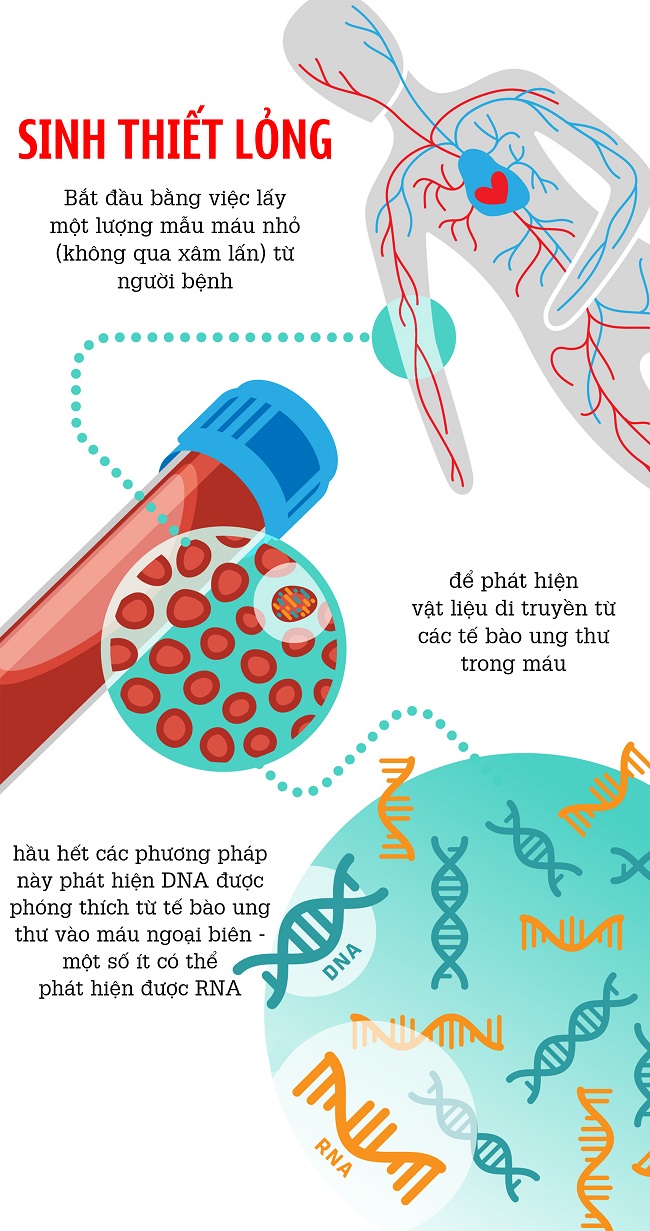
Gần đây, phương pháp Xét nghiệm không xâm lấn - Liquid biopsy (còn được gọi là Sinh thiết lỏng), dựa vào nguyên tắc phát hiện sự hiện diện của những phân mảnh DNA ngoại bào được phóng thích từ tế bào ung thư, khối u vào máu ngoại biên (Circulating tumor DNA - ctDNA), đã được chứng minh có tiềm năng ứng dụng trong chẩn đoán ung thư. Tuy nhiên, độ nhạy của phương pháp sinh thiết lỏng phụ thuộc vào lượng ctDNA được khối u phóng thích ra và rất khác biệt giữa các giai đoạn ung thư.
Nồng độ DNA trong huyết tương dưới 100 ng/mL, phần lớn là những đoạn cfDNA (Cell-free DNA) phân hủy do các quá trình sinh học của cơ thể như chết theo chu trình (apoptosis), hoại tử (necrosis). Ở bệnh nhân ung thư, ngoài DNA có nguồn gốc từ những quá trình trên, còn có DNA nguồn gốc từ tế bào ung thư chiếm một lượng nhỏ (~ 10%) trong tổng cfDNA. Các mảnh DNA này có chiều dài khoảng dưới 150bp, ngắn hơn so với các đoạn DNA có nguồn gốc từ tế bào thường (~ 160bp). Sự khác biệt về kích thước, vị trí trên hệ gene, các đặc điểm về di truyền ngoại gene (methyl hóa,…) là các đặc điểm quan trọng phát hiện. Ngoài ra, thời gian tồn tại trong máu của các ctDNA này là khoảng ngắn hơn 2 giờ, do vậy có thể phản ánh chính xác tình trạng tế bào ung thư tại thời điểm lấy mẫu. Với đặc điểm kích thước ngắn, chỉ chiếm lượng nhỏ trong cfDNA có trong mẫu máu/huyết thanh, việc phát hiện ctDNA bằng kĩ thuật Real-time PCR hay giải trình tự Sanger không hiệu quả. Với sự phát triển của các kỹ thuật hiện đại, việc phát hiện ctDNA được cải thiện độ nhạy, độ đặc hiệu và các phân tích về sau cũng được cải thiện. Hiện nay có hai nền tảng công nghệ cơ bản để phát hiện và đánh giá các ctDNA từ mẫu phẩm bao gồm PCR cải biên và giải trình tự gen thế hệ mới NGS (Next Generation Sequencing), cụ thể:
Ø PCR kỹ thuật số vi giọt (droplet digital PCR, ddPCR) sử dụng các giọt vi lỏng (microfluidic) khuếch đại các đoạn DNA bằng mồi huỳnh quang được thiết kế sẵn, hệ thống sẽ đọc tín hiệu kênh màu (tương tự như Real-time PCR) ;
Ø BEAMing (beads, emulsion, amplification and magnetic) là kĩ thuật kết hợp khuếch đại DNA bằng PCR nhũ hóa (emulsion PCR) và phân tích kết quả bằng phương pháp đếm tế bào dòng chảy (flow cytometry) ;
Ø Giải trình tự gen thế hệ mới NGS để khuếch đại lượng lớn các đoạn DNA ngắn có trong mẫu, phân tích và đối chiếu với các trình tự có sẵn để phát hiện những biến thể DNA đột biến điểm, đột biến cấu trúc, mức độ methyl hóa,…
CAPP-Seq (Cancer Personalized Profiling by deep Sequencing) thuộc nhóm phương pháp NGS, dựa trên sự bắt giữ để phát hiện ctDNA bằng cách sử dụng các mẫu dò chọn lọc DNA oligonucleotide được biotatin hóa để gắn đặc hiệu vào các trình tự DNA đích là các vùng bị đột biến thường xuyên trong từng loại ung thư cụ thể, cho phép xác định nhiều loại ung thư chỉ trong một lần chạy.
Theo một số nghiên cứu, ctDNA chiếm một phần nhỏ (< 1%) trong tổng DNA tự do hiện diện trong máu (cfDNA). Tuy nhiên, với các kỹ thuật phân tích hiện đại đã đạt được độ nhạy cao. Một ví dụ minh họa, ở bệnh nhân ung thư đại trực tràng (CRC), có thể phát hiện ctDNA dựa vào khối lượng khối u, có giới hạn phát hiện từ 50% (ở bệnh nhân không di căn) đến 90% (ở những bệnh nhân di căn). Ở những người đã phẫu thuật, việc phát hiện ctDNA sau khi mổ dao động từ 10 - 15% (bệnh nhân mắc bệnh giai đoạn II) đến gần 50% (bệnh nhân bị giai đoạn IV). Dựa trên những nghiên cứu này, các ứng dụng tiềm năng của ctDNA đang được phát triển nhanh trên nhiều loại ung thư, bao gồm cả CRC.
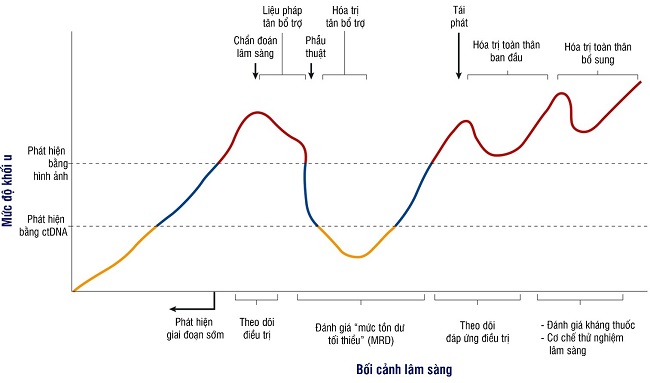
Sử dụng ctDNA có độ nhạy cao hơn so với phát hiện khối u bằng hình ảnh hoặc các kỹ thuật khác. Trong ung thư đại trực tràng, ctDNA phát hiện sớm khối u khi chưa có biểu hiện lâm sàng hoặc chụp X-quang, đánh giá "mức tồn dư tối thiểu, MRD". Ở bệnh nhân mắc bệnh (chụp X-quang), ctDNA cũng cho thấy độ nhạy hơn giúp theo dõi mức độ khối u, hỗ trợ điều chỉnh phát đồ điều trị. Bên cạnh đó, ctDNA hỗ trợ đánh giá sự phát triển, không đồng nhất của khối u dẫn đến kháng thuốc và lựa chọn phát đồ phù hợp.
Ví dụ về khả năng ứng dụng lâm sàng của ctDNA trong ung thư đại trực tràng
Bởi có vai trò quan trọng trong nghiên cứu và điều trị các bệnh lý, đặc biệt là các bệnh ung thư, ctDNA đang là vấn đề nghiên cứu quan tâm của các nhà khoa học, bác sĩ lâm sàng trên toàn thế giới. Năm 2022, Hiệp hội Ung thư Châu Âu đã đưa ra những phân tích, đánh giá, quy chuẩn tham khảo và các khuyến cáo chung liên quan tới ứng dụng sinh thiết lỏng và ctDNA trong các chẩn đoán, tiên lượng và điều trị ung thư.
Trong tương lai gần, ctDNA có thể được sử dụng để sàng lọc nguy cơ tái phát và nhận diện tái phát ung thư sớm hơn so với chụp X-quang. Sinh thiết lỏng có thể trở thành một phần của các xét nghiệm thường quy như cholesterol và đường huyết, giúp kiểm soát tốt hơn các bệnh nhân ung thư giai đoạn cuối và phát hiện ung thư ở giai đoạn sớm, giúp điều trị thành công cao. Phương pháp Sinh thiết là hứa hẹn ứng dụng để hỗ trợ bác sĩ trong việc chẩn đoán, tiên lượng và đưa ra phác đồ chữa trị phù hợp…
v Hãy cùng xem Infographic dưới dây để hiểu rõ hơn về Sinh thiết lỏng ctDNA.
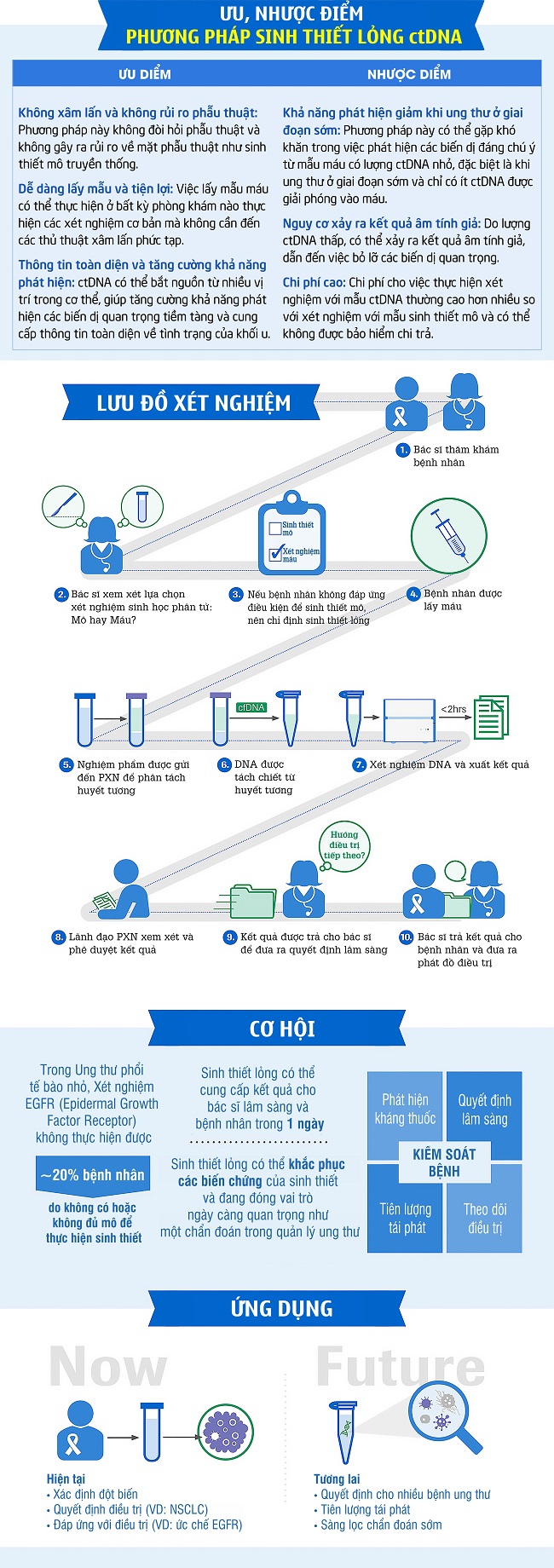
Thiên Chương
(Tổng hợp)
Tham khảo:
1. Aditi P. Singh, Haiying Cheng, Xiaoling Guo, Benjamin Levy, and Balazs Halmos (2017), Circulating Tumor DNA in Non–Small-Cell Lung Cancer: A Primer for the Clinician JCO Precision Oncology. 1, 1-13.
2. Bray, F., Laversanne, M., Sung, H., Ferlay, J., Siegel, R. L., Soerjomataram, I., & Jemal, A. (2024). Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, 74(3), 229-263.
3. Dasari, A., Morris, V.K., Allegra, C.J. et al. (2020), ctDNA application and integration in colorectal cancer: an NCI Colon and Rectal-Anal Task Forces whitepaper. Nat Rev Clin Oncol 17, 757-770.
4. Pascual J., Attard G., Bidard F.-C., Curigliano G., De Mattos-Arruda L., Diehn M., Italiano A., Lindberg J., Merker J., Montagut C., et al. (2022), ESMO recommendations on the use of circulating tumor DNA assays for patients with cancer: A report from the ESMO Precision Medicine Working Group. Ann. Oncol;33:750–768.
Các tin khác
- Công văn 4790/SYT-TCCB ngày 30/5/2024 của Sở Y tế về việc Hướng dẫn cập nhật kiến thức y khoa liên tục trong khám bệnh, chữa bệnh quy định tại Thông tư số 32/2023/TT-BYT ngày 31/12/2023 của Bộ trưởng Bộ Y tế (04/06/2024)
- Xét nghiệm máu giúp chẩn đoán sớm bệnh Alzheimer (30/05/2024)
- Ảnh hưởng của rượu, bia đối với hệ thần kinh (30/05/2024)
- Những điều cần biết về Bệnh sán dây và ấu trùng sán lợn (30/05/2024)
- “Vũ khí mới” của Ngành Y tế Thành phố Hồ Chí Minh trong chiến dịch phòng, chống sốt xuất huyết (24/05/2024)





